1.1 治療薬開発において注目される動向
新型コロナウイルス感染症(COVID-19)が世界で蔓延するなか、すでに承認されていたり、開発中である既存薬を新型コロナウイルス感染症治療薬に転用する開発が活発化している。
具体的には、「レムデシビル」(Gilead Sciences)、「アビガン」(富士フイルム富山化学)、「バリシチニブ」(Eli Lilly)などが挙げられる。これらは本来それぞれ別の疾患を対象とする治療薬であるが、新型コロナウイルス感染症の治療においても有効であるとして早期承認・実用化に向けた動きが進んでいる。
具体的には、「レムデシビル」(Gilead Sciences)、「アビガン」(富士フイルム富山化学)、「バリシチニブ」(Eli Lilly)などが挙げられる。これらは本来それぞれ別の疾患を対象とする治療薬であるが、新型コロナウイルス感染症の治療においても有効であるとして早期承認・実用化に向けた動きが進んでいる。
表1 開発中の新型コロナウイルス感染症治療薬(一部)
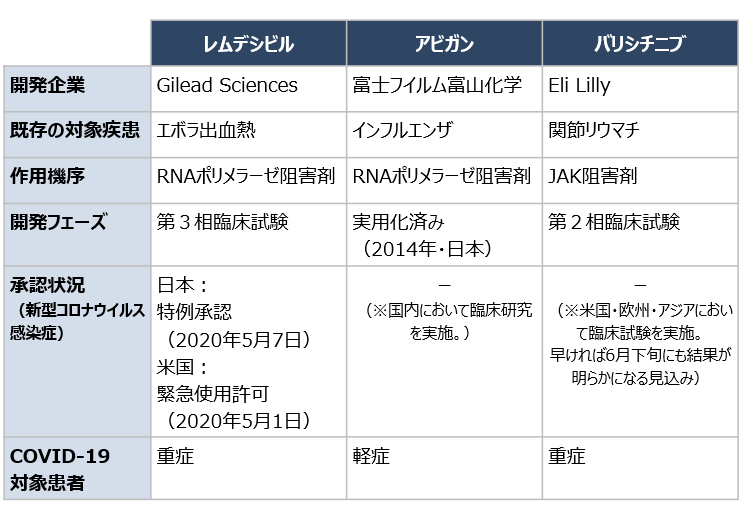
出所:三菱総合研究所作成
1.2 既存薬がなぜ効果があるのか
レムデシビル、アビガンはともに抗ウイルス薬で、RNAポリメラーゼというウイルスの複製に必要な酵素を阻害しウイルスの増殖を抑制する薬である。抗ウイルス薬の作用機序を図1に示す。
またバリシチニブは、炎症反応に関わるJAK(ヤヌスキナーゼ)酵素を阻害することで症状を抑える薬である。ウイルス感染後に引き起こされる過剰な炎症反応(サイトカインストーム)を抑制することで重症化を阻止する。(新型コロナウイルス感染症治療薬などに関する情報についてはコラム「ウィルス性感染症に関する基礎の基礎」でも記載。)
またバリシチニブは、炎症反応に関わるJAK(ヤヌスキナーゼ)酵素を阻害することで症状を抑える薬である。ウイルス感染後に引き起こされる過剰な炎症反応(サイトカインストーム)を抑制することで重症化を阻止する。(新型コロナウイルス感染症治療薬などに関する情報についてはコラム「ウィルス性感染症に関する基礎の基礎」でも記載。)
図1 抗ウイルス薬(レムデシビル、アビガン)が作用する仕組み
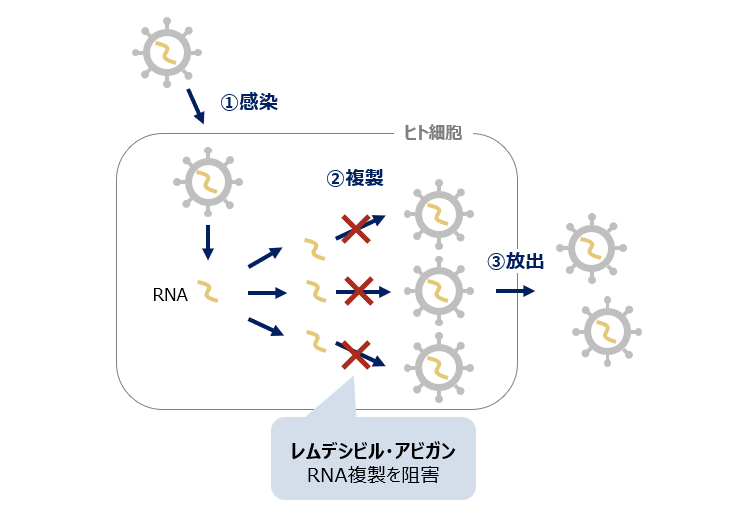
出所:三菱総合研究所作成